Invima autoriza ensayo clínico de la vacuna de Johnson & Johnson contra la COVID-19 en Colombia
- Francisco Rossi Buenaventura es nuevo director del Invima: ya había estado en la entidad
- Destituyen a 12 exfuncionarios del Invima por el caso de corrupción ‘Invima paralelo’
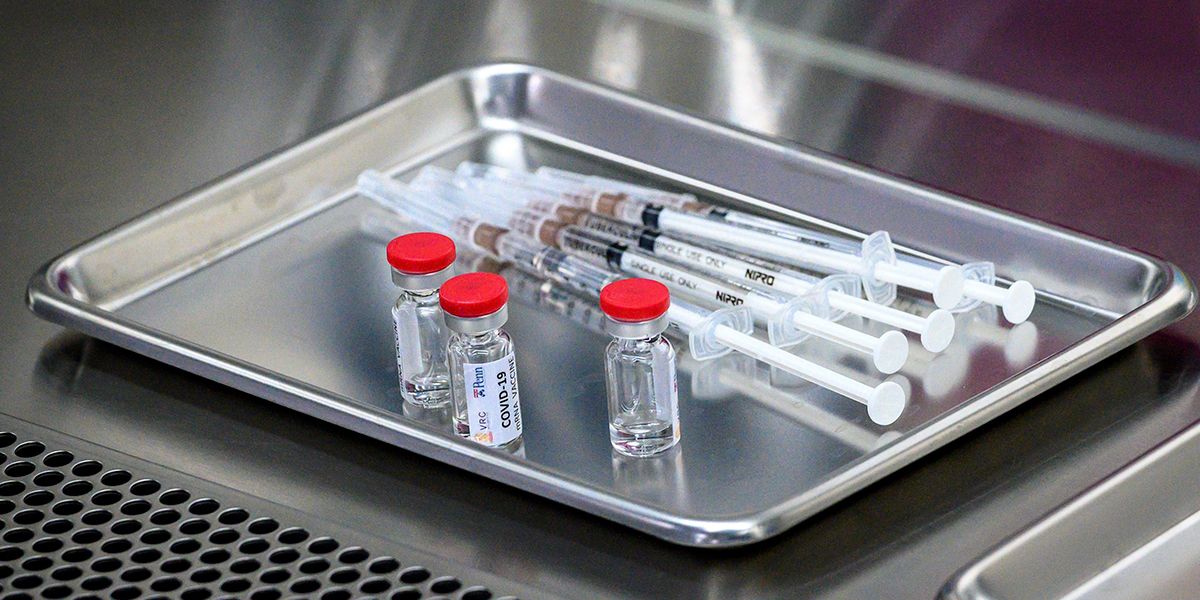
El Invima autorizó el ensayo clínico en Colombia de la vacuna Ad26.COV2.S, desarrollada por Janssen, la compañía farmacéutica de Johnson & Johnson, que busca combatir la COVID-19.
Se espera que Colombia esté lista para empezar el estudio fase III, una vez se presenten los resultados del estudio fase 1/2a en el mes de septiembre de 2020.
“La capacidad de la agencia sanitaria y las medidas adoptadas permitieron la materialización de una política pública en salud, ubicando a Colombia en el escenario mundial de países viables para iniciar los ensayos clínicos con estas vacunas”, expresó Julio César Aldana, director general del Invima.
Mire también: Colombia participará en ensayos clínicos de una vacuna de Johnson & Johnson contra la COVID-19
A nivel mundial, la Fase III se llevará a cabo, de manera competitiva, inicialmente en 6 países: Estados Unidos, Chile, Colombia, México, Perú y Sudáfrica, con una población total de 60.000 participantes.
Primer grupo de centros aprobados por el Invima
- Fundación Cardiovascular de Colombia – Bucaramanga
- Centro de Investigación Médico Asistencial S.A.S (CIMEDICAL S.A.S) – Barranquilla
- Centro de Atención e Investigación Médica S.A.S (CAIMED S.A.S) – Bogotá
- Fundación Hospital Universidad del Norte – Barranquilla
- Fundación Oftalmológica de Santander (FOSCAL) – Floridablanca
- Solano & Terront Servicios Médicos Ltda (UNIENDO) – Bogotá
El ensayo clínico se desarrollará en las siguientes etapas
- Etapa 1a: participantes (adultos entre 18 y 60 años) sin comorbilidades asociadas con un aumento en el riesgo de progresión a COVID-19 intenso
- Etapa 1b: participantes (adultos entre 18 y 60 años) con comorbilidades que se asocian con aumento del riesgo de progresión a COVID-19 intenso
Los interesados en participar deben de tener en cuenta
- La casa farmacéutica es quien define los países participantes en el estudio y los centros de investigación en los cuales se llevará a cabo.Ningún actor del Gobierno Nacional o Entidad Territorial de Salud define los criterios de elegibilidad de los participantes ni las características del ensayo clínico.
- Los criterios de inclusión y exclusión son establecidos a nivel global, por la compañía farmacéutica que desarrolla el medicamento/producto en investigación, y se pueden consultar en esta página web: www.clinicaltrials.gov
- Los criterios de inclusión y exclusión serán verificados por el médico especialista del centro de investigación, persona encargada de validar los datos, teniendo en cuenta la historia clínica del participante.
- Los participantes del ensayo clínico deben firmar un consentimiento informado.
- También deben cumplir a cabalidad cada una de las recomendaciones del equipo investigador.
- En Colombia está prohibido el pago y el uso de incentivos para los participantes por el hecho de vincularse a algún ensayo clínico aprobado.
La fecha estimada de inicio del estudio fase III para reclutar participantes es septiembre del 2020, y la fecha estimada de finalización primaria es marzo de 2023.



